服务中心
CUSTOMER SERVICE
间充质干细胞(MSCs)因其再生和分化能力在再生医学领域显示出巨大潜力。与骨髓来源的MSCs(BM-MSCs)相比,脐带组织来源的MSCs(HUC-MSCs)因易于获取且可大规模扩增,具有免疫调节和抗炎特性,增殖潜力高、分化能力强,免疫原性低、无伦理争议等优点备受关注。本文主要阐述了一项随机、双盲、安慰剂对照的I/II期临床试验,旨在评估HUC-MSCs静脉输注治疗老年衰弱患者的安全性和有效性。研究者对HUC-MSCs进行了流式细胞术分析,以下是本期应用精要对此文中流式实验部分的详细解读:
根据国际细胞治疗学会(ISCT)的标准,MSCs必须表达特定的表面标志物组合。该研究的流式实验主要用于鉴定和确认HUC-MSCs的表面标志物表达模式,这是MSCs质量控制的关键环节;同时也对研究中涉及的细胞因子变化进行详细评估。


CD73、CD90、CD105(阳性标志物)和CD11b、CD19、CD31、CD34、CD45、HLA-DR(阴性标志物)

样本处理:
临床级HUC-MSCs(第五代细胞)

质量控制:
实验按照GMP标准操作流程进行

细胞因子水平:
评估肿瘤坏死因子-α(TNF-α)、干扰素-γ(IFN-γ)、白细胞介素-8(IL-8)、白细胞介素-17(IL-17)的表达水平,分别在基线、1周、1个月、2个月、3个月和6个月的随访点进行了连续测量。


CD73、CD90和CD105表达阳性;
这些标志物是MSCs的特征性表面分子,参与细胞粘附、迁移和分化等过程。

阴性标志物表达:
CD11b(髓系标志物)、CD19(B细胞标志物)、CD31(内皮细胞标志物)、CD34(造血干细胞标志物)、CD45(白细胞共同抗原)和HLA-DR(MHC II类分子)均为阴性;
阴性结果排除了造血细胞、内皮细胞和免疫细胞的污染。

质量控制参数:
细胞活力>90%(符合释放标准);
无细菌、支原体、病毒等污染;
内毒素≤0.5 EU/mL。

细胞因子水平:
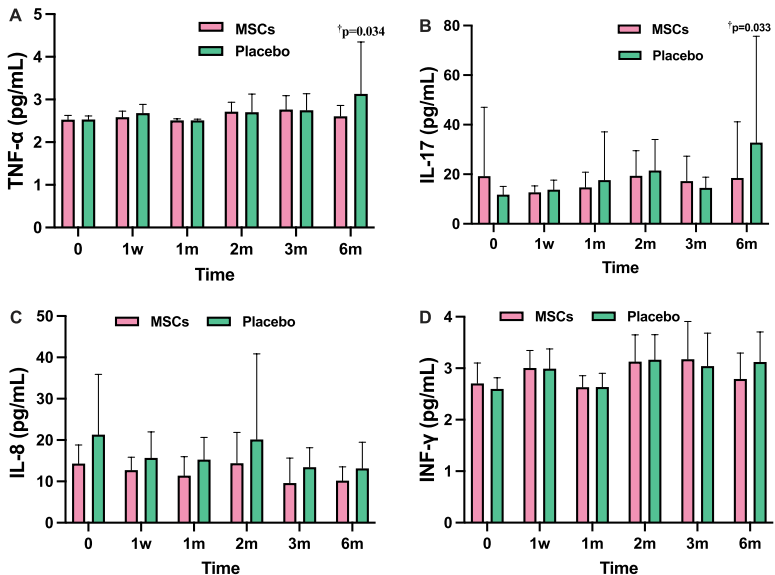
图 1. 细胞因子水平变化
TNF-α的变化:TNF-α是一种关键的促炎细胞因子,与肌肉减少症和虚弱密切相关。
在6个月随访时,MSCs组的TNF-α水平显著低于安慰剂组(p=0.034);
这种下降趋势从第2个月开始显现,并在6个月时达到统计学显著性;
TNF-α的降低与患者身体功能(如握力和步行速度)的改善相关。
IL-17的变化:IL-17是Th17细胞分泌的促炎细胞因子,参与慢性炎症过程。
在6个月随访时,MSCs组的IL-17水平显著低于安慰剂组(p=0.033);
IL-17的下降模式与TNF-α类似,但波动幅度更大;
这种变化表明MSCs可能调节了Th17细胞介导的炎症反应。
IL-8和IFN-γ的结果:与上述两种细胞因子不同,研究未发现IL-8和IFN-γ在两组间有显著差异。
IL-8水平在两组中都呈下降趋势,但组间差异不显著;
IFN-γ水平保持相对稳定,未观察到治疗相关变化。

层浪生物3光14色流式细胞仪LongCyte®在该研究中扮演了关键角色
🔺点击图片了解更多LongCyte®详情
1.国际标准符合性:
CD73、CD90、CD105 阳性表达,完全符合 ISCT 对 MSCs 的鉴定标准,确认细胞为间充质干细胞。
CD34、CD45(造血标志物)、CD31(内皮标志物)阴性,排除异源细胞污染,确保纯度;HLA-DR 阴性证实免疫原性低,支持异体移植安全性。
2.分化潜能证据:
通过番红 O 染色(软骨分化)、油红 O 染色(脂肪分化)、茜素红染色(成骨分化),验证 HUC-MSCs 的多向分化能力,补充质量控制维度。

1.抗炎机制验证:
治疗组 6 个月时 TNF-α(p=0.034)和 IL-17(p=0.033)水平显著下降,提示 MSCs 通过抑制 Th17 细胞介导的炎症通路,减轻慢性低度炎症。
炎症因子降低与握力、步行速度等身体功能改善正相关,佐证 “抗炎 - 功能修复” 的治疗逻辑。
2.临床转化基础:
细胞表型正确性为免疫调节、组织修复功能提供前提,与患者生活质量(SF-36 评分)提升的临床结果一致;
流式检测的 GMP 标准操作(细胞活力 > 90%、内毒素≤0.5 EU/mL)为规模化生产和临床推广奠定基础。

1.标准化操作体系:
严格遵循 ISCT 标志物检测标准,同时覆盖 6 项阴性标志物和 3 项阳性标志物,避免漏检风险;
临床级细胞(第 5 代)制备符合 GMP 规范,确保实验可重复性。
2.全面质量控制:
除表面标志物外,结合分化潜能检测、无菌检测(无细菌 / 支原体污染)和内毒素监测,形成多维质控体系;
流式分析结果与 “未出现严重不良事件” 的临床安全性数据相互印证,强化结论可信度。

这项研究首次证实HUC-MSCs治疗老年衰弱的安全性和有效性,为这一难治性疾病提供了新的治疗选择,并可观察到在改善生活质量、身体性能和减少慢性炎症方面的积极结果。HUC-MSCs来源广泛、易于扩增,提示HUC-MSC疗法在治疗老年衰弱方向具有较好的临床应用前景,同时为干细胞治疗老年衰弱提供了重要证据,为应对全球老龄化挑战提供了新的思路和方法。流式细胞术的质量控制也为后续临床试验的安全性和有效性结果提供了重要保障。
参考文献:
Zhu et al. Safety and efficacy of umbilical cord tissue-derived mesenchymal stem cells in the treatment of patients with aging frailty: a phase I/II randomized, double-blind, placebo-controlled study. Stem Cell Research & Therapy (2024) 15:122.
——END——